Garść aktualności z Bioceltix’a – ostatnie komunikaty i webinar dla inwestorów

25.01
Spółka uzyskała zgodę na Węgrzech na przeprowadzenie planowanego terenowego badania klinicznego weterynaryjnego na koniach z klinicznymi objawami zwyrodnienia stawów z wykorzystaniem badanego produktu leczniczego weterynaryjnego BCX-EM na bazie mezenchymalnych komórek macierzystych.
Dla przypomnienia całe badanie zostanie przeprowadzone na co najmniej 93 koniach w 4-5 wybranych krajach w maksymalnie 15 ośrodkach badawczych. Więc w najbliższym czasie można spodziewać się jeszcze kilku podobnych komunikatów.
Link do komunikatu
9.02
Informacja dotycząca aktualnego statusu realizacji zleconego weterynaryjnego pilotażowego badania klinicznego ukierunkowanego na zebranie danych o skuteczności produktu BCX-CM-AD przeznaczonego do leczenia atopowego zapalenia skóry u psów.
Z komunikatu dowiadujemy się, że rekrutacja pacjentów została zakończona. W badania łącznie bierze udział 30 zwierząt, podzielonych na dwie grupy – 20 w grupie, której podaje się produkt spółki oraz 10 w grupie z innym produktem dopuszczony do obrotu (grupa kontrolna).
Na dzień publikacji raportu 10 pacjentów z pierwszej grupy zakończyło badanie – u 9 pacjentów zaobserwowano oczekiwaną poprawę stanu klinicznego. Z kolei w grupie kontrolnej badanie zakończyło 3 pacjentów – u wszystkich zaobserwowano poprawę. Reszta pacjentów znajduje się w fazie obserwacji. Dodatkowo dowiadujemy się, że badanie zostanie wydłużone, ze względu na wykluczenie 2 zwierząt o około 6 tygodni.
Oczywiście zbyt wcześnie na wnioski o wadzę statystycznej, ale spółka określa dotychczasowe wynik jako „pozytywne i dobrze rokujące”.
Link do komunikatu
Webinar dla inwestorów
Wczoraj (9.02) również miało miejsce spotkanie spotkanie z zarządem. Na webinarze, poza przedstawieniem spółki oraz jej projektów, padło kilka ciekawych nowych lub zaktualizowanych informacji i właśnie na nich chcemy się skupić.
Spółka pracuje nad kluczowymi produktami leczniczymi: na zmiany zwyrodnieniowe stawów u psów, na atopowe zapalenie skóry u psów oraz zapalenia stawów u koni. Dla każdego nich został przedstawiony przejrzysty harmonogram prac. Warto się z nimi zapoznać, bo pozwalają się inwestorowi zorientować, gdzie prace nad danym produktem zmierzają oraz umiejscowić je na osi czasu. Oczywiście należy pamiętać, że pewne przesunięcia mogą tutaj mieć miejsce.

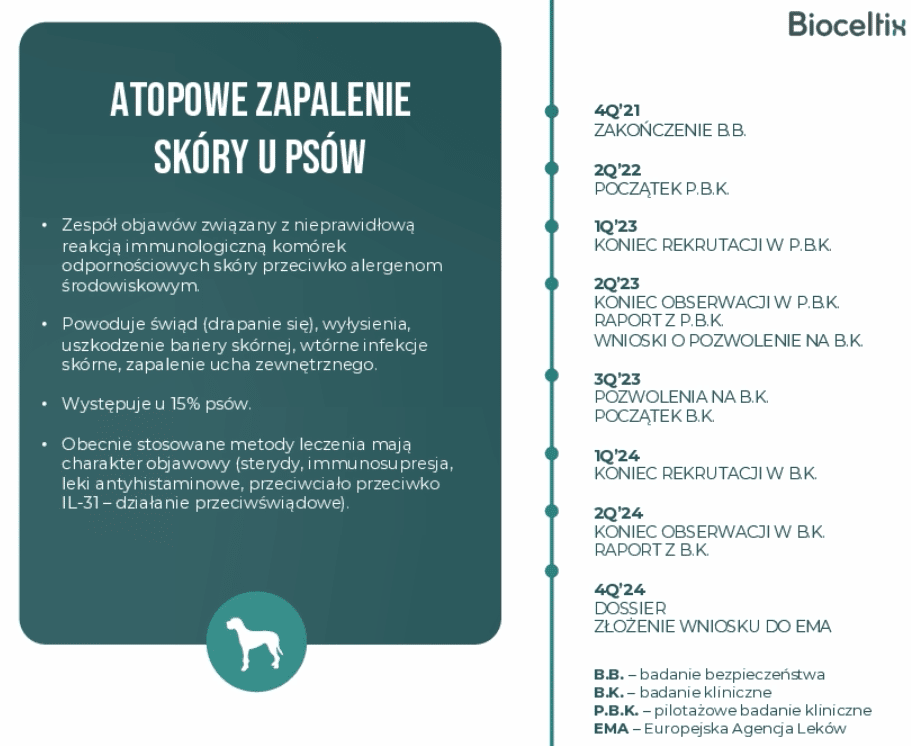

Jeszcze warto zauważyć, że poszczególne terminy przyszłych etapów nieco się różnią od prognozowanych terminów podczas GPW Innovation Day w czerwcu ubiegłego roku dla obu psich projektów i różnią się dość znacznie dla produktu końskiego (różnica w okolicy 1 roku). W odniesieniu do produktu końskiego, na usprawiedliwienie spółki trzeba wspomnieć, że to opóźnienie wynikało z próby uzyskania prawa do badań klinicznych przyśpieszoną ścieżką równolegle z badaniami bezpieczeństwa TAS. Terminy te zostały wpisane na wcześniejsze prezentacje, ale końcowo taki wariant nie doszedł do skutku, więc spółka musiała ukończyć badania TAS, a dopiero następnie zasadnicze badanie kliniczne. Gdyby spółka wpisała terminy z normalną, obecnie realizowaną procedurą, opóźnienie wcale by nie nastąpiło, lub byłoby minimalne, ponieważ samo badanie bezpieczeństwa TAS zakończyło się zgodnie z wcześniej założonym terminem.
Spółka przedstawiła ceny pierwszego zarejestrowanego leku na bazie komórek macierzystych
stosowanego w kulawiznie u koni -Arti-Cell Forte (opracowanego przez belgijskie Global Stem Cell Technology, a przejętego później przez Boehringer Ingelheim). Ceny różnią się w zależności od miejsca zakupu i wynoszą np. 1200 funtów za jedną dawkę w Wielkiej Brytanii, 2000 euro w Finlandii, co wskazuje, że jest to produkt „premium” jednoznacznie skierowany do bogatszego klienta. Zauważono również, że jego dostępność jest bardzo słaba, czego przyczyną, według zarządu, może być to, że opracowany model jest trudny do wyskalowania.
Paweł Wielgus zasygnalizował poślizg w badaniach klinicznych
produktu na zmiany zwyrodnieniowe stawów u psów (BCX-CM-J) oraz badania pilotażowego produktu na atopowe zapalenie skóry u psów (BCX-CM-AD). BCX-CM-AD ma zakończyć w drugim kwartale 2023, przy czym zaznaczono, że przesunięcie zakończenia badania pilotażowego nie wpłynie na termin rozpoczęcia właściwego badania klinicznego. BCX-CM-J zakończy się w trzecim kwartale 2023. Daty te oznaczają zakończenie obserwacji i ostateczne raporty z badań.
Przedstawiono cele na rok 2023,
znalazły się tam:
– zawarcie umowy partneringowej – w tym celu zawarto umowę z doradcą transakcyjnym ze Szwajcarii, który ma bardzo duże doświadczenie w transakcjach na rynku weterynaryjnym, który wspomoże spółkę w całym procesie
– zakończenie badania klinicznego produktu na zmiany zwyrodnieniowe stawów u psów
– złożenie dossier do EMA (Europejska Agencja Leków) dla produktu na zmiany zwyrodnieniowe stawów u psów
– rozpoczęcie badania klinicznego produktu na atopowe zapalenie skóry u psów oraz zapalenie stawów u koni
– wytwarzanie serii produktów do badań w standardzie GMP
– walidacja obecnego szlaku technologicznego (do dossier składanego do EMA)
– pozyskanie dotacji na badanie kliniczne produktu na atopowe zapalenie skóry u psów oraz jego rejestracje
– pozyskanie dotacji na badanie kliniczne produktu bezkomórkowego (sekretom)
– rozszerzenie ochrony patentowej
– emisja akcji – spodziewana jest na wiosnę tego roku, podczas spotkania nie zostały przedstawione żadne konkretne parametry
Spółką według nas zasługuje na bardzo dużą pochwałę za bardzo dobre relacje inwestorskie. Komunikuje się z rynkiem często, podczas prezentacji jasno przedstawia co się udało zrealizować z planu oraz gdzie wystąpiły problemy. Zaprezentowano konkretne cele na obecny rok i prośbę o ich rozliczenie za rok, a jeżeli inwestorzy będą sobie tego życzyć mogą robić spotkania nawet co kwartał. Życzylibyśmy sobie, żeby każda spółka miała taką politykę relacji inwestorskich ;).
Nowym elementem jest na pewno emisja akcji. Biocelitx do tej pory robił emisje mniejsze, ale za to częściej, sytuacja rynkowo nie była zbyt korzystna, a spółka nie chciała się zbytnio rozwadniać. Częste emisje dla polskie inwestora są dość bolesne i elementem, który na pewno „kłuje w oczy”. Jednak naszym zadanie spółka postąpiła bardzo słusznie. Wyobraźcie sobie, że Bioceltix zamiast robić małe emisje, robi jedną duża np. na 20 mln zł, przy kursie 30 zł i słabej sytuacji rynkowej. Jak duże dyskonto względem ceny rynkowej spółka musiałaby zaoferować i końcowo jak duże byłoby to rozwodnienie? W wariancie z kilkoma mniejszymi emisjami końcowo uzyskamy taką samą sumę, ale z mniejszym rozwodnieniem, co jest oczywiście korzystne dla każdego inwestora, ale nominalnie jest to „więcej emisji”. Właśnie gdyby spółka nie liczyła się kompletnie z inwestorami, zrobiłaby bardzo dużą emisji, niezależnie od ceny i rozwodnienia, byle tylko ściągnąć kasę. Dla samej spółki więcej emisji to tylko więcej pracy i zamieszania.